L’autotest VIH autorisé
Le Conseil national du sida (CNS) s’est prononcé dans un avis rendu public à leur mise à disposition en pharmacie, en parapharmacie mais aussi sur Internet. Le CNS répondait à une saisine de la ministre de la Santé qui, dans un courrier du 8 août 2012 fait explicitement référence à l’autotest salivaire de dépistage de l’infection à VIH autorisé en juillet 2012 aux États-Unis.
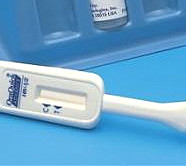
« Le 3 juillet dernier, l’agence américaine des médicaments (FDA) a autorisé la mise sur le marché d’un TROD VIH (Oraquick) en tant qu’autotest sans supervision médicale. Ce test sera en vente libre à partir d’octobre 2012 dans plus de 30 000 points de distribution aux États-Unis et il est très probable qu’on ne le retrouve après cette date, accessible sur Internet », écrit-elle. S’ils ne sont pas autorisés en Europe, les autotests les tests de dépistage avec auto-prélèvement capillaire à domicile sont disponibles légalement aux États-Unis depuis 1996.
La nouveauté est que le nouveau test Oraquick in Home HIV approuvé aux États-Unis a fait l’objet d’une évaluation approfondie qui a montré une amélioration des performances de l’autotest. Celui-ci présente une spécificité (capacité à donner un résultat négatif lorsque l’infection n’est pas présente) de 98 %, jugée satisfaisante, et une sensibilité (capacité à donner un résultat positif lorsque l’infection est présente) de 92,9 %. Cette sensibilité est « relativement moins satisfaisante » notamment en phase de primo-infection, relève le CNS qui souligne même qu’une étude réalisée par une équipe française a révélé une sensibilité encore moindre de 86,5 %. Toutefois, le rapport bénéfices/risques quelles que soient les hypothèses retenues, notamment concernant le niveau de sensibilité et l’apparition de faux négatifs, reste favorable.
Son introduction en France permettrait la première année de découvrir 4 000 nouvelles infections et d’en éviter 400.
















Commentaires récents